Nitrobenzeno
Nitrobenzeno | |||||
 | |||||
Plata kemia strukturo de la Nitrobenzeno | |||||
 | |||||
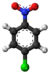
Tridimensia kemia strukturo de la Nitrobenzeno | |||||
Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | C6H5NO2 | ||||
| CAS-numero-kodo | 98-95-3 | ||||
| ChemSpider kodo | 7138 | ||||
| PubChem-kodo | 7416 | ||||
| Merck Index | 15,6674 | ||||
Fizikaj proprecoj | |||||
| Aspekto | senkolora aŭ duonflava likvaĵo | ||||
| Molmaso | 123,111 g·mol-1 | ||||
| Denseco | 1,1986g cm−3 | ||||
| Fandpunkto | 5,7°C | ||||
| Bolpunkto | 210,9°C | ||||
| Refrakta indico | n76120{displaystyle n_{761}^{20}} 1,5529 | ||||
| Ekflama temperaturo | 88 °C | ||||
| Memsparka temperaturo | 480 °C | ||||
| Acideco (pKa) | 3,98 | ||||
| Solvebleco | Akvo:Malmulte solvebla | ||||
| Mortiga dozo (LD50) | 350 mg/kg (buŝe) | ||||
Sekurecaj Indikoj | |||||
| Riskoj | R10 R23/24/25 R40 R48/23/24 R51/53 R62 | ||||
| Sekureco | S28 S36/37 S45 S61 | ||||
Pridanĝeraj indikoj | |||||
Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa | ||||
| GHS Deklaroj pri damaĝoj | H301, H311, H331, H336, H351, H360, H361, H372, H411, H412 | ||||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P260, P261, P264, P270, P271, P273, P280, P281, P301+310, P302+352, P304+340, P308+313, P311, P314, P321, P330, P361, P363, P391, P403+233, P405, P501[1] | ||||
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo (25 °C kaj 100 kPa) | |||||
Nitrobenzeno aŭ C6H5NO2 estas organika aromata kombinaĵo, senkolora aŭ duonflava likvaĵo, nesolvebla en akvo kun migdalosimila odoro, kiu frostiĝas donante duonverde flavaj kristaloj. Ĝi estas produktata larĝaskale kiel antaŭaĵo de anilino. En laboratorio, ĝi okaze uzatas kiel solvanto, ĉefe por elektrofilaj reakciantoj[2].
Nitrobenzene estis unue izolita de Mitscherlich en 1834 kaj ĝi plenumas gravan industrian rolon. Komerce ĝi estas vendata kiel artefarita oleo de amaraj migdaloj sub la nomo de mirbanoleo.[3]
En 1847, la brita kemiisto Charles Mansfield (1819-1855) unue patentigis kaj komerce produktis ĝin por parfumfabrikado sub la nomo de Oleo de Mirbano. Pro ĝia aromataj proprecoj kaj migdalosimila odoro, ĝi iĝis malmultekosta esencaĵo uzata en beleco-produktoj kiel porman- kaj vizaĝ- kremoj kaj domsapoj kaj eĉ en dolĉajoj, marcipanoj kaj likvoroj.[4]
Enhavo
1 Sintezoj
1.1 Sintezo 1
1.2 Sintezo 2
2 Reakcioj
2.1 Reakcio 1
2.2 Reakcio 2
2.3 Reakcio 3
3 Literaturo
4 Referencoj
Sintezoj |
Sintezo 1 |
- Preparado per interagado de nitrogena duoksido kaj benzeno:
2 |
Sintezo 2 |
Klorobenzeno reakcias kun natria nitrito por formi nitro-benzenon kaj natrian kloridon:
|
Reakcioj |
Reakcio 1 |
- Preparado de anilino per reduktado de nitrobenzeno:[5]
|
Reakcio 2 |
- Nitrobenzeno reakcias kun amonia klorido kaj zinko por formi fenil-hidroksil-aminon, zinkan kloridon, akvon kaj amoniakon:[6]
|
Reakcio 3 |
- Nitrobenzeno reakcias kun klorgaso por formi p-nitro-klorobenzenon:
|
Literaturo |
- Aniline Production from Nitrobenzene
- Encyclopedia of Chemical Processing and Design
- Synthetic and Mechanistic Organic Electron Transfer Reactions
- Nitrobenzenes—Advances in Research and Application
- Information Technology and Agricultural Engineering
- Handbook of Commercial Catalysts: Heterogeneous Catalysts
Referencoj |
↑ PubChem
↑ Elektrofilaj reakciantoj estas kemiaj substancoj kiuj altiras elektrojn.
↑ Competition Science Vision
↑ Fashion Victims: The Dangers of Dress Past and Present
↑ Nitrobenzene
↑ Competition Science Vision









![{displaystyle {mathsf {{xrightarrow[{60^{o}C}]{HNO_{3}+H_{2}SO_{4}}},}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec4c6a66dc99e8219982a4a680a7230457d488e0)
 +
+
 +
+![{displaystyle {mathsf {{xrightarrow[{,}]{}},}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)
![{displaystyle {mathsf {{xrightarrow[{}]{}},}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)
 +2
+2 +2
+2 +
+ +
+